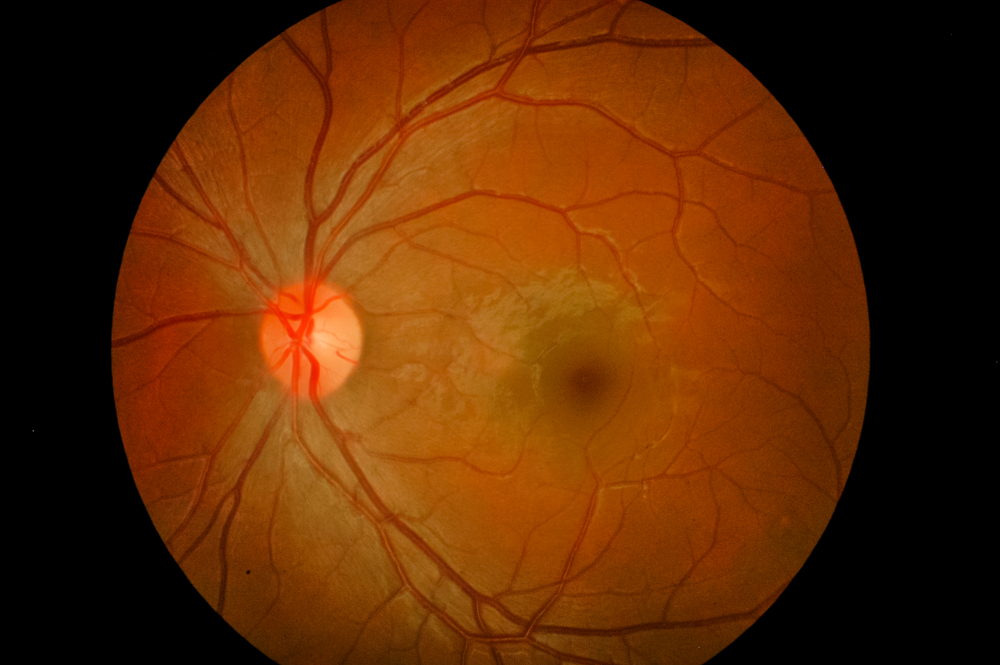
La dégénérescence maculaire liée à l’âge touche plus de 200 millions de personnes dans le monde. On peut distinguer la DMLA sèche et la DMLA humide, la forme sèche constituant la majorité des patients, tandis que la DMLA humide est considérée comme plus agressive et entraîne de graves déficiences visuelles. L’un des premiers symptômes est une vision floue, où les lignes droites semblent déformées. Cela peut se traduire par de l’obscurité, des blancs ou des zones floues au centre du champ de vision. La DMLA est l’une des principales causes de cécité irréversible dans le monde. Bien que certaines thérapies retardent la perte de la vision centrale, aucun traitement actuel ne la rétablit complètement.
Une croissance vasculaire anormale dans l’œil peut entraîner une dégénérescence maculaire liée à l’âge
Des scientifiques du système de santé de l’Université de Virginie ont identifié une nouvelle cible pour prévenir la formation d’enchevêtrements anormaux de vaisseaux sanguins associés à des maladies oculaires telles que la dégénérescence maculaire liée à l’âge néovasculaire, la rétinopathie diabétique proliférative et l’ischémie.
L’étude a ouvert la possibilité d’atténuer la croissance anormale des vaisseaux sanguins dans les maladies oculaires en ciblant la machinerie épigénétique. En ciblant localement le régulateur épigénétique, les chercheurs ont mieux compris comment les cellules immunitaires oculaires peuvent provoquer une perte de contrôle de la croissance des vaisseaux sanguins sous la rétine. Cette approche offre également une nouvelle orientation pour le développement d’interventions plus efficaces et moins coûteuses, évitant ainsi des questions telles que la résistance aux médicaments, qui est un problème croissant avec les thérapies anti-VEGF traditionnelles utilisées dans les traitements cliniques.
Les scientifiques savaient déjà que la croissance anormale des vaisseaux dans l’œil est alimentée par des quantités excessives d’une substance appelée facteur de croissance endothélial vasculaire A, ou VEGF, qui joue un rôle important dans la formation des vaisseaux sanguins. La nouvelle recherche identifie une protéine clé qui détermine les niveaux de VEGF. Le blocage de cette protéine chez des souris de laboratoire a permis de réduire de manière significative et ciblée leur taux de VEGF, sans effets secondaires indésirables. Par exemple, les scientifiques ont constaté qu’elle n’avait aucun effet toxique sur la rétine, la partie de l’œil sensible à la lumière où se produit la prolifération vasculaire. Cette découverte répond à une question de longue date sur la façon dont les cellules immunitaires oculaires telles que les macrophages contribuent à la croissance anormale des vaisseaux sanguins sous la rétine.
En plus d’identifier une cible prometteuse pour le développement de nouveaux traitements contre la perte de vision, cette découverte jette une lumière importante sur les mécanismes fondamentaux responsables de la prolifération des vaisseaux sanguins qui rend aveugles des millions de personnes. Bien qu’il faille encore beaucoup de recherches et de tests avant que les nouvelles découvertes puissent être traduites en un traitement, les scientifiques sont enthousiasmés par le potentiel de cette découverte.
Le rôle des cellules immunitaires dans le développement de la dégénérescence maculaire liée à l’âge
Lorsque nous vieillissons, le système immunitaire vieillit lui aussi.Auparavant, des scientifiques de la Washington University School of Medicine à St. Louis avaient découvert que le vieillissement des cellules immunitaires augmentait le risque de dégénérescence maculaire liée à l’âge, l’une des principales causes de cécité. En étudiant des souris et des cellules de patients, les chercheurs ont découvert que les cellules immunitaires appelées macrophages vieillissent et sont plus susceptibles de contribuer à l’inflammation et à la croissance anormale des vaisseaux sanguins qui endommagent la vision dans la dégénérescence maculaire. Leurs conclusions ont été publiées dans la revue JCI Insight.
Lors d’expériences sur des souris, l’équipe a découvert que les macrophages plus âgés portaient de plus grandes quantités de petits bouts de matériel génétique appelés microARN, qui contrôlent la façon dont les cellules expriment les gènes. Les chercheurs ont trouvé des niveaux significativement plus élevés de microARN-150 dans les macrophages des yeux des souris âgées. Les microARN aident à réguler de nombreuses choses dans les cellules en se liant à plusieurs gènes pour affecter la façon dont ces gènes fabriquent des protéines. Dans cette étude, les chercheurs ont découvert que dans un modèle murin de dégénérescence maculaire, le microARN-150 semblait orienter les macrophages plus âgés vers la promotion de l’inflammation et la formation de vaisseaux sanguins anormaux. Les chercheurs ont également testé des échantillons de sang de personnes atteintes ou non de dégénérescence maculaire. Les échantillons de patients atteints de dégénérescence maculaire présentaient également des niveaux significativement plus élevés de microARN-150 dans leurs macrophages.
Les thérapies de la dégénérescence maculaire visent à traiter les symptômes de la maladie plutôt que d’en traiter la cause. En comprenant ce qui arrive aux cellules immunitaires de l’œil, il pourrait être possible de développer des thérapies pour aider les patients qui ne peuvent pas être aidés par les médicaments existants. Si l’on parvient à réduire les niveaux de microARN dans les macrophages ou à modifier une ou plusieurs voies moléculaires régulées par ce microARN, on pourrait potentiellement réduire l’inflammation et perturber la croissance anormale des vaisseaux sanguins dans l’œil.
Une certaine protéine joue un rôle clé dans de nombreuses maladies liées à l’âge
Une recherche publiée dans le Physical Journal suggère qu’une protéine clé du sang est impliquée dans la cause de la dégénérescence maculaire et d’autres maladies liées à l’âge comme la maladie d’Alzheimer et l’athérosclérose. Il existe des centaines de protéines dans notre sang, mais les chercheurs se sont concentrés sur la vitronectine, l’une des plus abondantes. La vitronectine ne circule pas seulement en forte concentration dans le sang, mais aussi dans les échafaudages entre les cellules et est également un composant important du cholestérol. Cette protéine est une cible importante pour la dégénérescence maculaire car elle s’accumule au fond de l’œil et entraîne une perte de vision. Des dépôts similaires se produisent dans le cerveau dans le cas de la maladie d’Alzheimer et dans les artères dans le cas de l’athérosclérose.
Grâce à une analyse biochimique détaillée, les chercheurs ont découvert que la protéine peut subtilement changer de forme sous l’effet de la pression. Ces changements lui permettent de se lier plus facilement aux ions calcium présents dans le sang, ce qui, selon les chercheurs, entraîne la formation de dépôts de plaques calcifiées caractéristiques de la dégénérescence maculaire et d’autres maladies liées à l’âge. Ces connaissances structurelles simplifieront le développement de traitements contre la dégénérescence maculaire en permettant aux chercheurs de concevoir des anticorps sur mesure qui bloquent sélectivement la liaison de la protéine au calcium sans interférer avec ses autres fonctions importantes dans l’organisme.
L’obésité peut provoquer la dégénérescence maculaire liée à l’âge
Une étude canadienne publiée dans la revue Science révèle un autre mécanisme moléculaire susceptible de déclencher la dégénérescence maculaire liée à l’âge (DMLA). Les recherches menées à l’Hôpital Maisonneuve-Rosement de Montréal montrent comment les facteurs de stress de la vie, comme l’obésité, reprogramment les cellules du système immunitaire, les rendant destructrices pour l’œil au fur et à mesure que nous vieillissons.
On sait déjà que le système immunitaire de l’œil d’une personne atteinte de DMLA devient déréglé et agressif. Normalement, les cellules immunitaires maintiennent l’œil en bonne santé, mais l’exposition à des agents pathogènes tels que les bactéries et les virus peut les endommager. Parallèlement, les cellules immunitaires sont également activées lorsque le corps est exposé à des facteurs de stress, tels que l’excès de graisse dans l’obésité, ce qui fait de l’obésité le premier facteur de risque non génétique de développement de la DMLA.
Dans leur étude, les chercheurs ont utilisé l’obésité comme modèle pour accélérer et exagérer les facteurs de stress que le corps subit tout au long de la vie. Ils ont découvert que l’obésité transitoire, ou des antécédents d’obésité, entraînent des changements persistants dans l’architecture de l’ADN au sein des cellules immunitaires, ce qui les rend plus vulnérables à la production de molécules inflammatoires. Ces résultats fournissent des informations importantes sur la biologie des cellules immunitaires à l’origine de la DMLA et pourraient permettre le développement de traitements plus adaptés à l’avenir.