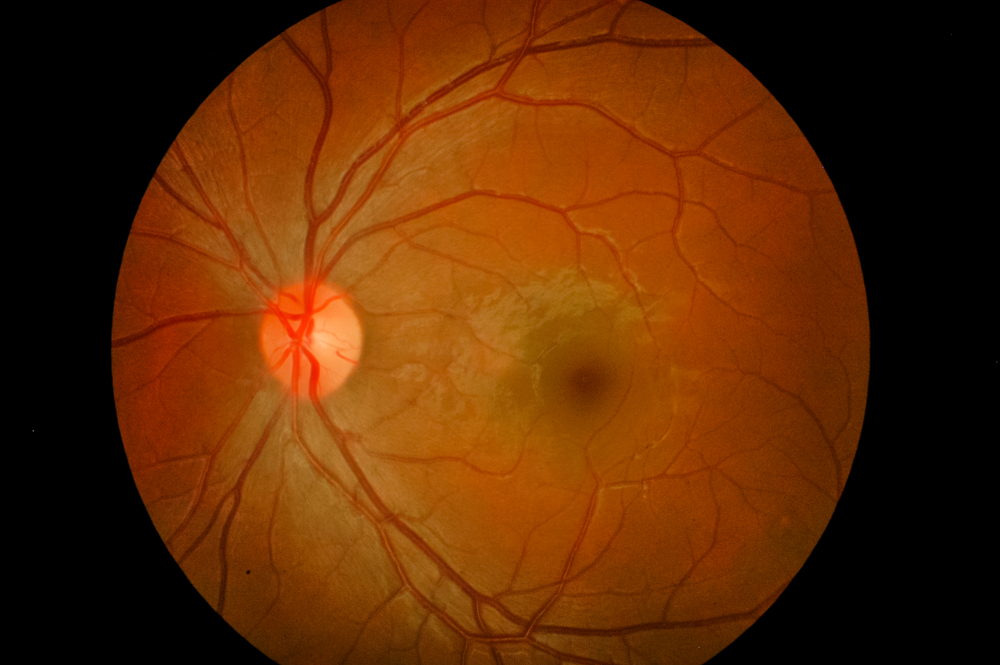
La degenerazione maculare legata all’età colpisce più di 200 milioni di persone in tutto il mondo. Si può distinguere tra AMD secca e umida: la forma secca costituisce la maggior parte dei pazienti, mentre l’AMD umida è considerata più aggressiva e porta a gravi danni alla vista. Un sintomo precoce è la visione sfocata, in cui le linee rette appaiono distorte. Questo può provocare oscurità, whiteout o aree sfocate al centro del campo visivo. L’AMD è una delle principali cause di cecità irreversibile in tutto il mondo. Sebbene alcune terapie ritardino la perdita della visione centrale, nessun trattamento attuale la ripristina completamente.
Una crescita vascolare anomala nell’occhio può portare alla degenerazione maculare senile
Gli scienziati dell’University of Virginia Health System hanno identificato un nuovo bersaglio per prevenire la formazione di grovigli anomali di vasi sanguigni associati a malattie oculari come la degenerazione maculare neovascolare legata all’età, la retinopatia diabetica proliferativa e l’ischemia.
Lo studio ha aperto la possibilità di mitigare la crescita anomala dei vasi sanguigni nelle malattie dell’occhio prendendo di mira il meccanismo epigenetico. Intervenendo localmente sul regolatore epigenetico, i ricercatori hanno acquisito una comprensione più approfondita di come le cellule immunitarie oculari possano causare una perdita di controllo sulla crescita dei vasi sanguigni nella retina. Questo approccio fornisce anche una nuova direzione per lo sviluppo di interventi più efficaci e meno costosi, evitando così problemi come la resistenza ai farmaci, che sono un problema crescente con le terapie anti-VEGF tradizionali utilizzate nei trattamenti clinici.
Gli scienziati sapevano già che la crescita anomala dei vasi sanguigni nell’occhio è alimentata da quantità eccessive di una sostanza chiamata fattore di crescita endoteliale vascolare A, o VEGF, che svolge un ruolo importante nella formazione dei vasi sanguigni. La nuova ricerca identifica una proteina chiave che determina i livelli di VEGF. Il blocco di questa proteina nei topi di laboratorio ha ridotto significativamente i livelli di VEGF in modo mirato, senza effetti collaterali indesiderati. Ad esempio, gli scienziati hanno scoperto che non ha effetti tossici sulla retina, la parte dell’occhio sensibile alla luce dove avviene la proliferazione vascolare. Questa scoperta risponde a una domanda di vecchia data su come le cellule immunitarie oculari, come i macrofagi, contribuiscano alla crescita anomala dei vasi sanguigni sotto la retina.
Oltre a identificare un bersaglio promettente per lo sviluppo di nuovi trattamenti per la perdita della vista, la scoperta getta una luce importante sui meccanismi fondamentali responsabili della crescita eccessiva dei vasi sanguigni che acceca milioni di persone. Anche se saranno necessarie molte altre ricerche e test prima che le nuove scoperte possano essere tradotte in un trattamento, gli scienziati sono entusiasti del potenziale della scoperta.
Il ruolo delle cellule immunitarie nello sviluppo della degenerazione maculare senile
Quando invecchiamo, anche il sistema immunitario invecchia. In precedenza, gli scienziati della Washington University School of Medicine di St. Louis avevano scoperto che l’invecchiamento delle cellule immunitarie aumenta il rischio di degenerazione maculare senile, una delle principali cause di cecità. Studiando topi e cellule di pazienti, i ricercatori hanno scoperto che le cellule immunitarie chiamate macrofagi invecchiano e hanno maggiori probabilità di contribuire all’infiammazione e alla crescita anomala dei vasi sanguigni che danneggiano la vista nella degenerazione maculare. I risultati sono stati pubblicati sulla rivista JCI Insight.
Negli esperimenti condotti sui topi, il team ha scoperto che i macrofagi più anziani contengono quantità maggiori di brevi frammenti di materiale genetico chiamati microRNA, che controllano il modo in cui le cellule esprimono i geni. I ricercatori hanno trovato livelli significativamente più elevati di microRNA-150 nei macrofagi degli occhi dei topi anziani. I microRNA aiutano a regolare molte cose nelle cellule legandosi a più geni per influenzare il modo in cui questi geni producono le proteine. In questo studio, i ricercatori hanno scoperto che in un modello murino di degenerazione maculare, il microRNA-150 sembra dirigere i macrofagi anziani a promuovere l’infiammazione e la formazione di vasi sanguigni anomali. I ricercatori hanno anche analizzato campioni di sangue di persone con e senza degenerazione maculare. Anche i campioni dei pazienti con degenerazione maculare presentavano livelli significativamente più elevati di microRNA-150 nei macrofagi.
Le terapie per la degenerazione maculare mirano a trattare i sintomi della malattia piuttosto che la causa. Comprendendo cosa accade alle cellule immunitarie nell’occhio, potrebbe essere possibile sviluppare terapie per aiutare i pazienti che non possono essere aiutati con i farmaci esistenti. Se si riuscisse in qualche modo a ridurre i livelli di microRNA nei macrofagi o ad alterare una o più vie molecolari regolate da questo microRNA, si potrebbe potenzialmente ridurre l’infiammazione e interrompere la crescita anomala dei vasi sanguigni nell’occhio.
Una certa proteina svolge un ruolo chiave in molte malattie legate all’età
Una ricerca pubblicata sul Physical Journal suggerisce che una proteina chiave presente nel sangue è coinvolta nella degenerazione maculare e in altre malattie legate all’età come l’Alzheimer e l’aterosclerosi. Nel sangue sono presenti centinaia di proteine, ma i ricercatori si sono concentrati sulla vitronectina, una delle più abbondanti. La vitronectina non solo circola in alte concentrazioni nel sangue, ma anche nell’impalcatura tra le cellule ed è anche un componente significativo del colesterolo. Questa proteina è un bersaglio importante per la degenerazione maculare, perché si accumula nella parte posteriore dell’occhio e porta alla perdita della vista. Depositi simili si verificano nel cervello nel morbo di Alzheimer e nelle arterie nell’aterosclerosi.
Attraverso un’analisi biochimica dettagliata, i ricercatori hanno scoperto che la proteina può cambiare sottilmente forma sotto pressione. Questi cambiamenti la portano a legarsi più facilmente agli ioni di calcio presenti nel sangue, il che, secondo i ricercatori, porta alla formazione dei depositi di placche calcificate caratteristici della degenerazione maculare e di altre malattie legate all’età. Queste conoscenze strutturali consentiranno di semplificare lo sviluppo di trattamenti per la degenerazione maculare, permettendo ai ricercatori di progettare anticorpi su misura che blocchino selettivamente il legame con il calcio della proteina senza interferire con altre sue importanti funzioni nell’organismo.
L’obesità può causare la degenerazione maculare senile
Uno studio canadese pubblicato sulla rivista Science scopre un altro meccanismo molecolare che può innescare la degenerazione maculare legata all’età (AMD). Una ricerca condotta presso l’Hôpital Maisonneuve-Rosement di Montreal mostra come fattori di stress della vita, come l’obesità, riprogrammino le cellule del sistema immunitario, rendendole distruttive per gli occhi quando si invecchia.
È già noto che il sistema immunitario nell’occhio di una persona affetta da AMD diventa disregolato e aggressivo. Normalmente, le cellule immunitarie mantengono l’occhio sano, ma l’esposizione ad agenti patogeni come batteri e virus può danneggiarle. Allo stesso tempo, le cellule immunitarie si attivano anche quando l’organismo è esposto a fattori di stress, come l’eccesso di grasso nell’obesità, rendendo l’obesità il primo fattore di rischio non genetico per lo sviluppo dell’AMD.
Nel loro studio, i ricercatori hanno usato l’obesità come modello per accelerare ed esagerare i fattori di stress a cui l’organismo è sottoposto nel corso della vita. Hanno scoperto che l’obesità transitoria, o una storia di obesità, porta a cambiamenti persistenti nell’architettura del DNA all’interno delle cellule immunitarie, rendendole più vulnerabili a produrre molecole infiammatorie. Questi risultati forniscono informazioni importanti sulla biologia delle cellule immunitarie che causano l’AMD e potrebbero consentire lo sviluppo di trattamenti più personalizzati in futuro.