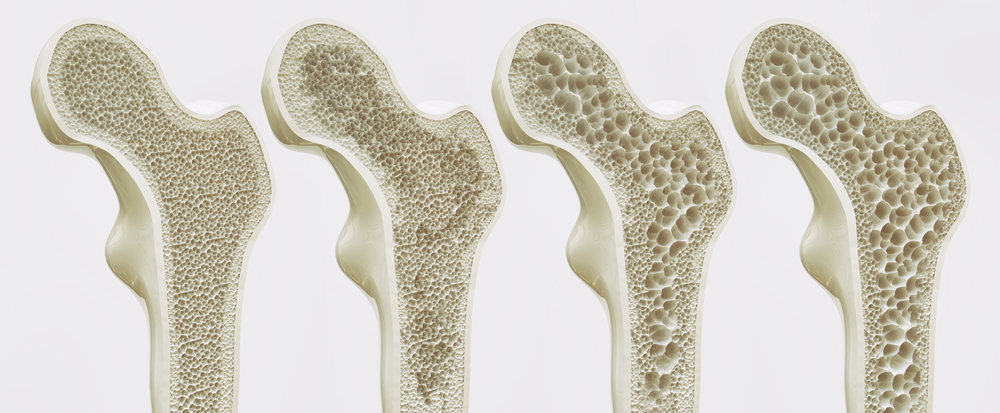
L’osteoporosi è la più comune malattia ossea legata all’età e colpisce centinaia di milioni di persone in tutto il mondo. Si stima che una donna su tre e un uomo su cinque di età superiore ai 50 anni soffrano di fratture ossee osteoporotiche. Alcuni fattori di rischio per l’osteoporosi, come l’età avanzata e il sesso femminile o una storia familiare di questa malattia, sono inalterabili. Tuttavia, i fattori negativi dello stile di vita, come il fumo, il consumo di alcol, l’assunzione di determinati farmaci o l’esposizione a inquinanti ambientali, possono essere evitati.
L’osteoporosi è causata da un’eccessiva attività delle cellule che assorbono l’osso, mentre l’attività delle cellule che lo formano è ridotta. Nelle persone sane, un processo strettamente controllato bilancia l’attività degli osteoblasti, che costruiscono l’osso, e degli osteoclasti, che lo demoliscono. Tuttavia, secondo una nuova ricerca, i danni ai mitocondri delle cellule possono causare un’alterazione di questo processo. I risultati fanno luce su come l’esposizione al fumo di sigaretta, all’alcol e ad alcuni farmaci e tossine ambientali possa aumentare il rischio di osteoporosi.
I mitocondri influenzano la salute delle ossa
Lo studio, condotto da ricercatori della Penn School of Veterinary Medicine, rivela un meccanismo che potrebbe collegare questi fattori all’osteoporosi. Il danneggiamento dei mitocondri – importanti organismi cellulari e generatori di energia – porta a un aumento della formazione di cellule chiamate osteoclasti, responsabili della perdita di tessuto osseo. Questi effetti sono stati rilevati sia in colture cellulari sia in modelli animali. Un’alterata funzione mitocondriale non solo ha un impatto negativo sulla produzione di energia, ma innesca anche una sorta di segnale di stress che induce la sovrapproduzione di osteoclasti.
Per capire come il danno mitocondriale possa essere collegato all’osteoporosi attraverso il lavoro dei macrofagi, i ricercatori hanno indotto un danno a un enzima chiave responsabile della produzione di energia nei mitocondri, la citocromo ossidasi C, in macrofagi di topo cresciuti in laboratorio. Questo ha fatto sì che i macrofagi rilasciassero una serie di molecole di segnalazione associate a una risposta infiammatoria e sembrava anche incoraggiarli a intraprendere il percorso verso gli osteoclasti.
Quando hanno osservato da vicino cosa stava accadendo, hanno notato un’anomalia con una molecola chiave, RANK-L, che aiuta a regolare il processo di costruzione dell’osso e viene rilasciata dalle cellule che lo costruiscono per indurre il riassorbimento osseo. Quando i mitocondri erano danneggiati, erano soggetti a segnali di stress e si convertivano in osteoclasti molto più velocemente, anche quando i livelli di RANK-L erano bassi. Questi osteoclasti portavano a tassi più elevati di riassorbimento osseo.
I ricercatori hanno confermato le loro scoperte in un modello murino e hanno dimostrato che gli animali con una mutazione che porta a mitocondri disfunzionali avevano una maggiore produzione di osteoclasti. Inoltre, i loro macrofagi presentavano livelli più elevati di fagocitosi, il processo con cui le cellule immunitarie inglobano e “mangiano” gli invasori. I ricercatori ritengono che questa maggiore capacità fagocitica possa essere responsabile di alcuni degli altri problemi fisiologici che possono verificarsi nelle persone con difetti nei mitocondri.
Poiché alcuni degli stessi fattori di rischio ambientali che sembrano promuovere l’osteoporosi, come il fumo e alcuni farmaci, possono anche influenzare la funzione mitocondriale, i ricercatori ritengono che questi segnali di stress possano essere la via attraverso la quale influenzano la salute delle ossa. Studi futuri potrebbero indagare su come preservare la funzione mitocondriale protegga dall’osteoporosi.
Gli emicanali Cx43 sono essenziali per il rafforzamento delle ossa
Le attività fisiche che sottopongono l’osso a stress meccanico stimolano la crescita di nuovo osso. Gli osteociti, che costituiscono il 90-95% di tutte le cellule ossee, aiutano a rilevare le sollecitazioni meccaniche sull’osso. Regolano quindi la disgregazione dell’osso indebolito da parte di cellule chiamate osteoclasti e la costruzione di nuovo osso da parte di cellule chiamate osteoblasti. Ricerche passate hanno già dimostrato che le sollecitazioni meccaniche sull’osso aumentano il numero di canali sulla superficie degli osteociti, chiamati emicanali della connexina (Cx) 43. In un nuovo studio, gli scienziati hanno voluto scoprire il ruolo di questi canali nella risposta alle sollecitazioni meccaniche sull’osso.
Per farlo, hanno studiato due tipi di topi. In uno, le connessioni tra le cellule ossee chiamate giunzioni gap erano compromesse, ma gli emicanali Cx43 erano rafforzati. Nell’altro, sia le giunzioni gap che gli emicanali Cx43 erano compromessi. L’équipe ha poi testato cosa succede alle ossa di questi topi, così come a quelle dei topi normali, quando vengono sottoposte a stress meccanico. Hanno scoperto che una sostanza chimica chiamata prostaglandina (PGE2) veniva prodotta sia nei topi tipici sia in quelli con giunzione gap compromessa in risposta allo stress meccanico, e le loro ossa diventavano più forti. Questa risposta era invece assente nei topi con emicanale Cx43 danneggiato.

Per confermare che gli emicanali Cx43 sono essenziali per il rafforzamento delle ossa, il team ha somministrato ai topi tipici un anticorpo che bloccava l’attività degli emicanali Cx43. Hanno scoperto che questo impediva agli animali di rilasciare PGE2 e riduceva la forza delle ossa in risposta a uno stress meccanico. Ma trattando gli stessi topi con PGE2 si ripristinavano gli effetti di rafforzamento osseo dello stress meccanico.
I trattamenti esistenti per l’osteoporosi sono generalmente mirati agli osteoclasti, che demoliscono l’osso indebolito, e agiscono riducendo il turnover osseo. Questo può inavvertitamente portare a ossa più fragili nel tempo ed è stato collegato ad alcuni rari ma gravi effetti collaterali. Questa ricerca dimostra che il bersaglio dei canali inibitori Cx43 sugli osteociti potrebbe essere un’opzione terapeutica alternativa che utilizza la risposta dell’organismo alle sollecitazioni meccaniche. Questa scoperta potrebbe aiutare gli scienziati a sviluppare nuovi trattamenti per l’osteoporosi o altre condizioni che contribuiscono alla perdita di massa ossea nei pazienti.
Nuove strategie di trattamento dell’osteoporosi
La maggior parte delle attuali terapie per l’osteoporosi prevede l’uso di bifosfonati, che bloccano l’attività delle cellule che assorbono l’osso, impedendone l’eccessivo riassorbimento. Tuttavia, il trattamento prolungato con questi farmaci elimina il necessario rimodellamento osseo, portando a un aumento del rischio di fratture e ad altri effetti collaterali indesiderati. Pertanto, è urgente sviluppare nuove strategie che superino i limiti dei trattamenti attuali. Ci sono nuovi progressi in quest’area.
Utilizzando analisi genetiche in un piccolo pesce da laboratorio, il medaka giapponese (Oryzias latipes), i ricercatori hanno identificato una piccola proteina, la chemochina CXCL9, che in condizioni di osteoporosi si diffonde verso i serbatoi contenenti precursori di cellule che assorbono l’osso. Questi precursori producono un recettore, CXCR3, sulla loro superficie cellulare. In seguito all’attivazione da parte di CXCL9, i precursori vengono mobilitati e migrano in modo altamente direzionale per lunghe distanze verso la matrice ossea, dove iniziano il riassorbimento osseo.
Sia CXCL9 che il suo recettore CXCR3 sono noti da tempo per modulare la migrazione delle cellule immunitarie verso i siti di infiammazione, ad esempio nella psoriasi e nell’artrite reumatoide. Esistono diversi inibitori chimici che bloccano l’attività del CXCR3, che hanno avuto scarso successo negli studi clinici per il trattamento della psoriasi. Il team di ricerca ha dimostrato che questi inibitori sono molto efficaci nel bloccare il reclutamento di cellule che riassorbono l’osso e nel proteggere l’osso dal danno osteoporotico.
La nuova strategia consente una modulazione fine del numero di osteoclasti reclutati nella matrice ossea, anziché un blocco generalizzato dell’attività degli osteoclasti come avviene nelle terapie convenzionali. Ciò comporta notevoli vantaggi, in quanto è possibile mirare e prevenire l’eccessivo riassorbimento osseo, pur mantenendo il normale turnover osseo. Ciò offre la possibilità di prevenire l’aumento del rischio di fratture nei pazienti affetti da osteoporosi e di mantenere un osso sano per migliorare la qualità della vita.